
- 所有服务
- 生命科学服务平台
- 诊断原料开发服务平台
- 抗体药物研发服务平台
LiP-MS靶点垂钓技术:生命科学领域的革新力量
在生命科学研究的前沿领域,质谱技术与结构生物学的深度交融,正悄然重塑药物靶点发现的范式。传统靶点垂钓方法往往需要对小分子进行复杂的化学修饰,这不仅耗费大量时间和精力,还可能干扰小分子的天然生物活性,从而影响研究结果的准确性。与之形成鲜明对比的是,限制性酶解-质谱联用技术(Limited Proteolysis-Mass Spectrometry,LiP-MS)凭借其免标记、高分辨率的独特优势,迅速崛起为探索药物-靶点相互作用的关键利器。
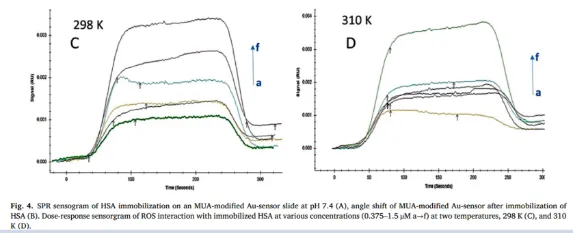
技术原理:捕捉分子结合的细微信号 LiP-MS技术的核心逻辑源于一个精妙的生物学现象:当小分子配体特异性结合到靶蛋白上时,会引发靶蛋白构象发生微妙变化,进而增强其空间结构的稳定性。这种构象变化会直接反映在蛋白酶切割位点的可及性上。该技术采用双重酶解策略,先利用蛋白酶K对样本进行有限酶解,随后使用胰蛋白酶进行完全消化。通过对比实验组与对照组的肽段丰度差异,能够将小分子在靶蛋白上的结合区域精准定位到12个氨基酸的尺度,且无需对小分子进行任何修饰,充分保留其天然活性。 实验流程:严谨科学的探索路径 LiP-MS实验是一个环环相扣的系统工程,涵盖蛋白提取、小分子-蛋白孵育、有限酶解与质谱分析等多个关键环节。在数据分析阶段,借助LiP-Quant框架整合剂量-响应曲线、蛋白频率库等多种特征,可准确计算靶点的置信度。同时,研究人员还会通过CETSA、SPR等多种技术手段对潜在靶点进行交叉验证,确保研究结果的可靠性。在紫堇灵抗胰腺纤维化的研究中,科研团队正是通过LiP-MS技术筛选出PSMA2作为潜在靶点,并通过基因敲低实验,从细胞学层面证实了该靶点的功能。
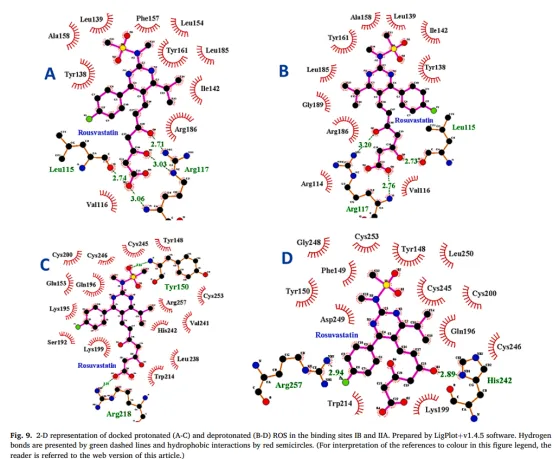
前沿应用:解锁生命奥秘的新钥匙 在肿瘤代谢研究领域,针对结直肠癌的研究中,LiP-MS成功锁定了油酸和异胆酸的直接靶点——烯醇化酶ENO1和脆性X相关蛋白FXR1,为揭示肿瘤代谢重编程机制提供了全新视角。在神经退行性疾病研究方面,通过分析小鼠脑脊液,LiP-MS发现了6种高置信度的神经退行相关蛋白,其中YWHAB和YWHAZ被证实可作为阿尔茨海默症的早期诊断标志物。 技术特性:优势与挑战并存 LiP-MS技术具有免标记检测、高空间分辨率、适用弱亲和力互作以及样本兼容性强等显著优势。然而,该技术也面临着一些挑战,如假阳性结果的控制、膜蛋白覆盖度较低以及低丰度蛋白检测困难等问题。不过,研究人员已经探索出一系列优化策略,如采用多剂量设计、在裂解缓冲液中添加去垢剂等,以提升技术的可靠性和适用性。
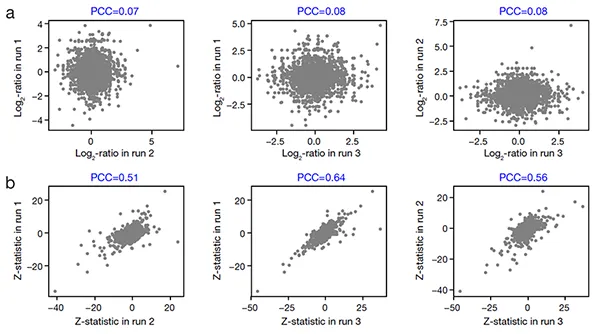
未来展望:迈向智能化与集成化 随着人工智能技术的蓬勃发展,LiP-MS有望与AlphaFold2预测模型和图神经网络分析深度结合,实现AI辅助的靶点预测。同时,通过与多组学数据的整合以及单细胞分析技术的融合,LiP-MS将进一步深化我们对细胞内化学通讯机制的理解,朝着药物靶点发现通用平台的方向不断迈进,为攻克“不可成药”靶点难题带来新的曙光。
研锦生物可以利用基于靶点或小分子结构的药物设计方法,对可购买化合物、天然产物等数据库进行虚拟筛选,并获得潜在活性的化合物列表供进一步活性实验确证。面向制药企业和科研院所,可提供一站式的早期药物研发服务,包括虚拟药物筛选、先导优化、靶标预测、 动力学模拟等,涉及小分子化学药、生物药、中药等多种新药类型,为您提供优质的药物发现服务
