温州医科大学和南京中医药大学研究人员发现中药蟾酥活性成分蟾毒灵的抑癌靶点
蟾酥(Bufonis Venenum.,蟾蜍的皮肤干燥分泌物)作为一种重要的中药,被广泛用于治疗多种疾病。例如,中华大蟾蜍皮经过加工制成的水溶性制剂—华蟾素,是我国临床上常用的一种中药抗肿瘤制剂,被中国国家食品药品监督管理局批准用于肺癌、结肠癌、胰腺癌等。蟾毒灵(bufalin)是蟾酥的主要单体活性成分,具有显著的肿瘤作用,然而其水溶性差、口服利用率低,毒性大、半衰期短等缺点限制了它的临床应用。因此,改善蟾毒灵的药代动力学特征,延长其作用时间,提高其疗效和减小毒副作用对扩展其临床应用至关重要。
现在为大家分享来自温州医科大学和南京中医药大学的2篇文章在改善蟾毒灵毒性上做出的重要工作,分别合成了蟾毒灵前药乙酰蟾毒灵(Acetyl-bufalin)和蟾毒灵结构功能类似物KU-177,显著改善蟾毒灵的药代动力学特征和疗效,并利用20K人类蛋白质组芯片阐明其作用靶点和作用机制。
01 乙酰蟾毒灵抑制非小细胞肺癌作用靶点及机制
2021年2月,温州医科大学药学院赵承光副研究员、附属第一医院王良兴教授及黄晓颖教授团队在British Journal of Cancer(IF=7.640)发表题为“Acetyl-bufalin shows potent efficacy against non-small-cell lung cancer by targeting the CDK9/STAT3 signaling pathway”的研究成果,自主创新设计合成了蟾毒灵前药—乙酰蟾毒灵(Ac-bu),并阐明了其作用靶点及作用机制。
研究人员首先为了解决蟾毒灵的代谢缺陷,设计合成了蟾毒灵的前药Ac-bu(图1A),细胞实验发现,Ac-bu对非小细胞肺癌细胞毒性较低且显著抑制细胞增殖(图1B),促进细胞凋亡(图1C)、诱导G2/M细胞周期停滞(图1D)、抑制STAT3信号通路(图1E),动物实验发现,Ac-bu显著提高肿瘤小鼠存活率(图1B)。

图1乙酰蟾毒灵的非小细胞肺癌治疗作用
Ac-bu的作用靶点及机制是什么呢?研究人员进行了20K人类蛋白质组芯片分析发现细胞周期依赖性蛋白激酶9(CDK9)与其结合力最强(图2A),分子对接显示Ac-bu与CDK9的ASP104、CYS106、ASP109残基形成3个氢键(图2B)。细胞实验发现,Ac-bu及SNS(CDK9抑制剂)均可显著抑制CDK9蛋白表达,并抑制STAT3信号通路激活(图2C),进一步Co-IP发现CDK9可以和STAT3相互结合形成复合体进而激活STAT3(图2D)。最后通过动物实验发现乙酰蟾毒灵和SNS可显著抑制肿瘤生长(图2E)。总之,乙酰蟾毒灵可抑制CDK9/STAT3信号轴发挥抗非小细胞肺癌的作用。
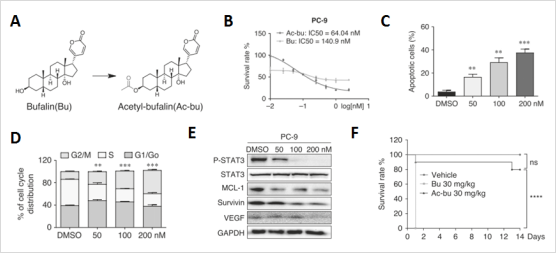
图2乙酰蟾毒灵作用靶点及机制
02 蟾毒灵及KU-177抑制多发性骨髓瘤的作用靶点及机制
2022年1月,南京中医药大学医学院杨烨、顾春艳教授团队在Journal of Experimental & Clinical Cancer Research(IF=11.161)发表题为“AHSA1 is a promising therapeutic target for cellular proliferation and proteasome inhibitor resistance in multiple myeloma”的研究成果,发现蟾毒灵直接作用靶点AHSA1并合成AHSA1选择性抑制剂KU-177。
研究人员首先采用20K人类蛋白质组芯片发现AHSA1与Bufalin结合力最强(图3A),随后发现AHSA1与多发性骨髓瘤(Multiple myeloma,MM)存活率正相关(图3B、C),微型热泳(Microscale thermophoresis,MST)验证显示Bufalin与AHSA1直接结合(图3D),深入机制研究揭示AHSA1作为HSP90A的协同伴侣激活CDK6和PSMD2,从而促进MM细胞增殖、耐药(图3E、F、G),而Bufalin能够干扰AHSA1和HSP90之间的相互作用会降低CDK6和PSMD2的表达,进而抑制细胞增殖和耐药(图3H)。
图3蟾毒灵发挥MM治疗作用靶点及机制
鉴于Bufalin是一种剧毒但有效的抗癌化合物,研究人员合成了AHSA1选择性抑制剂KU-177(图4A),分子对接显示K137A是AHSA1的活性位点(图4B),MST验证显示AHSA1的K137A突变后降低与KU-177的结合能力(图4C)。细胞、动物实验显示KU-177和Bufalin有着相同的作用机制(图4D),且KU-177与蛋白酶体抑制剂药物联合用药显示出良好抗肿瘤活性(图4E)。总之,KU-177可特异性靶向AHSA1,作为HSP90A的协同伴侣激活CDK6和PSMD2,从而促进MM细胞增殖、耐药(图4F)。

图4 化合物KU-177的MM治疗靶点及机制
总结与讨论
两篇研究在“以毒攻毒”治疗恶性肿瘤的中医药理论启发下,以具有抗肿瘤活性的传统毒性中药蟾酥提取物---Bufalin为线索,立足于传统中医药理论与资源,综合运用20K人类蛋白质组芯片、蛋白质谱等方法,筛选并鉴定了Bufalin的新靶标以及先导化合物,避免了Bufalin直接应用引起的毒副作用,最终达到了“减毒增效”的目的。
案例1:直接优化Bufalin,发现Acetyl-bufalin具有更好的疗效和更低的毒副作用,并通过20K人类蛋白质组芯片发现它的直接作用靶点CDK9,继而发现抑制CDK9/STAT3信号轴发挥抑制非小细胞肺癌的作用机制。
案例2:通过20K人类蛋白质组芯片发现Bufalin的直接作用靶点AHSA1及AHSA1作为HSP90A的协同伴侣激活CDK6和PSMD2从而促进MM以后,针对该靶点开发了与蟾毒灵的靶点和作用机制相同但疗效更好毒性更低的化合物KU-177。
总之,两篇文章充分体现了中药活性成分是创新药物的重要来源,发现其作用靶点对揭示中药理论的物质基础,开发更好的低毒高效的药物至关重要。
研锦生物专注于先导化合物、抗体药物、药物靶点的发掘;其次也为靶向药物筛选提供前期CRO服务,面向全球科研院所、高校、医院以及药企等科研机构。公司主要有以下平台:计算机辅助药物设计平台;SPR药物动力学检测平台;重组蛋白、抗体表达平台;以及细胞动物检测药效、毒理等实验平台;致力于靶向药物的前期开发筛选。

